Von Innen nach Außen planen
Wie bei fast allen Planungsvorhaben stehen am Anfang die gleichen Fragen:
- welche Produkte sollen hergestellt werden und in welchen Mengen?
- welche Prozesse sind dafür erforderlich?
- was sind die Nutzeranforderungen für diese Prozesse?
Aus diesen Planungsgrundlagen lassen sich dann ermitteln:
- welche Maschinen und Anlagen man in welcher Größe und Anzahl für den Prozess benötigt;
- wie viel Personal für den Prozess einzuplanen ist;
- welches und wie viel Material in die Herstellungsprozesse hinein- und in welcher Form und Menge wieder herausgeht.
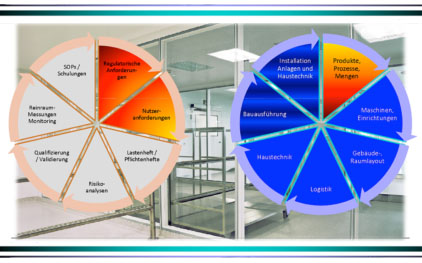
Daraus lassen sich nun die benötigten Flächen und Volumina für die Prozessanlagen, die Personalräume, die Lager und Materialflussflächen ermitteln und dann das Raum-Layout für diese Bereiche gestalten. Der blaue Regelkreis oben auf der Seite stellt diese Planungs- und Ausführungsstufen dar.
Im reglementierten GMP-Umfeld sind jedoch zusätzlich zu beachtende Faktoren von essenzieller Bedeutung: alle Maßnahmen, welche die EU-GMP-Regularien vorschreiben, um die Betriebs- oder Herstellungserlaubnis zu erhalten. Diese Maßnahmen sind im grauen Regelkreis dargestellt und beinhalten im wesentlichen:
- Erstellung von Lastenheften, welche die Nutzeranforderungen beschreiben und als Basis für die zu erstellenden Pflichtenhefte (vom Lieferanten zu erstellen) dienen
- Durchführung von Risikoanalysen im Rahmen eines umfassenden Risiko-Management-Prozesses; Integration der als kritisch erkannten Punkte in die weitere Planung
- Berücksichtigung aller regulatorischen Anforderungen in der Planung und Ausschreibung; dazu gehören im Wesentlichen:
- Entwicklung eines auf die Produktanforderungen abgestimmten Hygienekonzeptes
- Entwicklung eines auf das Hygienekonzept abgestimmtes Druckstufenkonzept zur Sicherung der Raumdruckkaskade
- Entwicklung eines GMP-konformen, cross-contamination-vermeidenden Personal- und Materialfluß
- detaillierte Vorgaben an Ausführung und Hygienic Design aller reinraumumschließenden Komponenten wie Wände, Boden, Decken, Türen, Fenster und Verfugungsmaterialien (Wussten Sie, dass es speziell getestetes und zertifiziertes Reinraumsilikon gibt?)
- detaillierte Vorgaben an Ausführung und Hygienic Design aller Einbauten im Reinraum, wie Elektro- und Sanitärinstallationen, Regale und Schränke, Materialdurchreichen, Lüftungs- und MSR-Komponenten, Monitoringinstallationen, IT-Installationen und natürlich an die Prozessanlagen und Hilfsgeräte
Wissen Sie, dass GMP-Bereiche kontinuierlich gemonitort werden müssen, welche Kriterien hierbei überwacht und welche Anforderungen an GAMP-konforme Monitoringsysteme gestellt werden? Wissen Sie, welche Anschlüsse für wiederkehrende Reinraum-Messungen wo und in welcher Form eingeplant werden müssen? Wissen Sie, welchen Anforderungen Schleuseneinrichtungen in Reinräumen entsprechen müssen und dass für eine optimale Funktion diese speziell auf die Anzahl Personen, Bevorratungsmengen und der Kleidung entsprechend dem Hygienekonzept angepasst werden müssen?
- detaillierte Vorgaben an die TGA-Planung in Bezug auf benötigte Medien wie Rein- und Reinstwasser, Gase, Vakuum, Absaugungen und deren Integration in die RLT-Planung
Sind diese zusätzlichen GMP-Anforderungen nicht bereits in Ihrer Ausschreibung berücksichtigt, ist der Konflikt mit den Reinraum-Gewerken schon vorprogrammiert. Das Ergebnis sind dann kostspielige Nachträge, Umbauten oder Probleme in der Abnahme durch die Aufsichtsbehörden.
-

Edelstahltisch in Hygienic Design in einem Reinraum Klasse B (Fotos: Fr. Sailer GmbH)
-

Deckenbündiger FFU mit Drallauslass und Gläserne Rückluftkanäle mit Reinigungstür (Fotos: Ritterwand)
Behörden-Management ist bei GMP-Projekten noch wichtiger als bei sonstigen Gewerbe-Objekten.
Ein Reinraum der von der Aufsichtsbehörde keine Betriebserlaubnis erhält, darf nicht genutzt werden und ist damit häufig erst nach kostspieligen Umbauten nutzbar. Ist der Reinraum für die termingerechte Einführung eines neuen Produktes vorgesehen, so kann selbst eine Terminverzögerung die beabsichtigte Nutzung in Frage stellen und hohe Verluste zur Folge haben.
Wir erstellen für GMP-Projekte grundsätzlich Prä-Qualifizierungsunterlagen, anhand derer wir der Zulassungsbehörde das Projekt unmittelbar nach der Phase der Entwurfsplanung vorstellen. Dadurch können erforderliche Änderungen noch kostengünstig einfließen und die spätere Abnahme und Erteilung der Betriebserlaubnis ist nicht gefährdet.
Die Prä-Qualifizierungsunterlagen müssen alle Informationen zu Prozessen, Anlagen und Maschinen, Layout, Haustechnik und allen qualitätssichernden Maßnahmen enthalten.
Was nicht in der Ausschreibung steht, ist nicht im Angebot
Diese leidvolle Erfahrung gilt für GMP- und Reinraumprojekte wie für alle sonstigen Gewerke. Auf Grund der Komplexität von Reinraumgewerken ist eine sorgfältige und vollständige Beschreibung aller Anforderungen noch wichtiger als bei normalen Projekten.
Reinraumprojekte können funktional oder über Leistungsverzeichnisse ausgeschrieben werden, die funktionale Ausschreibung überwiegt aktuell noch. Wie bei anderen Ausschreibungen ist auch hier eine der ersten Frage: Wie zieht man optimal die Schnittstellen:
- GU-Ausschreibung?
- Ausschreibung in Einzelgewerken?
- Bündelung stark voneinander abhängender Funktionalitäten zur späteren Vermeidung der Klärung von Gewährleistungen, z.B. gemeinsame Vergabe von Reinraumwänden, – decke, RLT-Anlage und MSR?
Wissen Sie, welche Vorgaben Sie in Bezug auf die Hygienestufen während des Baufortschrittes und welche Anforderungen Sie an die begleitende Baureinigung stellen müssen?
Selbstverständlich muss die Ausschreibung alle Informationen enthalten, aus der ein Unternehmer sein Angebot kalkulieren kann. Dies beinhaltet entweder die ausführliche funktionale Beschreibung des Vorhabens mit allen dazugehörigen Plänen, Raumlisten, Spezifikationen und sonstigen Vorbemerkungen und Randbedingungen oder die Ergänzung in Form eines Leistungsverzeichnisses. Zusätzlich erforderlich sind aber auch noch alle Vorgaben in Bezug auf die qualitätssichernden Maßnahmen:
- Lastenhefte und Validierungsmasterplan als Bestandteil der Ausschreibung Wissen Sie, welche Informationen ein Validierungsmasterplan enthält?
- Detaillierte Vorgaben zu Material, Oberflächen und Hygienic Design aller reinraumumschließenden Komponenten auf der Basis der Anforderungen der EU-GMP-Richtlinie
Wissen Sie, welche Anforderungen an Dichtungen und Schmiermittel bei Einsatz im Reinraum zu stellen sind? - Detaillierte Vorgaben zu Material, Oberflächen und Hygienic Design aller Reinraumeinbauten, Anlagen, Geräte und sonstiger Hilfsmittel
Wissen Sie, dass es „Cleanroom tested device“ gibt, wo Sie diese Informationen finden und wie diese Informationen zu bewerten sind? - Detaillierte Vorgaben zu Bauaufsicht, Baureinigung, Hygienemassnahmen während der Bauphasen
Wissen Sie, ob es einen Unterschied macht, ob auf Reinraumbaustellen mit Besen oder Staubsaugern gereinigt wird? Wie viele Stufen der Grundreinigung sind zu berücksichtigen? - Detaillierte Vorgaben zu Pflichtenheft, Mitwirkung bei den Risikoanalysen, Durchführung oder Mitwirkung bei Qualifizierungsschritten und Anforderungen an die qualifizierungsrelevante technische Dokumentation
Wissen Sie, welche technischen Dokumente für die Qualifizierung zusätzlich geliefert werden müssen? - Vollständiger Verweis auf alle einschlägigen Regelwerke zu Reinraum und Hygiene
Wissen Sie, welche Normen und Richtlinien den Stand der Technik im Reinraumbau beschreiben? Infos hierzu finden Sie am Ende dieses Artikels
Ist dieses Handwaschbecken nun GMP-konform?
![]()
Handwaschbecken dürfen/sollen nach der EU-GMP-Richtlinie in den unreinen Bereichen der ersten Personal- und Materialschleusen installiert werden. Um das Risiko einer Produktkontamination mit Partikeln oder Keimen zu minimieren, dürfen diese Installationen keine Kontaminationsquellen darstellen. GMP-Richtlinie, Pkt. 3.37: „Die zum Waschen und Reinigen verwendete Ausrüstung sollte so gewählt und eingesetzt werden, dass sie selbst keine Quelle der Verunreinigung darstellt.“
GMP-Richtlinie, Annex 1, Pkt. 46: „In reinen Bereichen sollen alle exponierten Oberflächen glatt, undurchlässig und ohne Risse sein…….und die wiederholte Anwendung von Reinigungs- und Desinfektionsmitteln zu ermöglichen.“
GMP-Richtlinie, Annex 1, Pkt. 47: „Um …. das Reinigen zu erleichtern, sollten keine unzugänglichen Nischen …….. vorhanden sein.“
Eine weitere Hygieneanforderung finden wir in der DIN EN 1672-2 „Nahrungsmittelmaschinen: Gestaltungsrichtlinien für hygienegerechtes Design“ sowie dem EHEDG Doc. 8: „Gestaltungskriterien für hygienegerechte Maschinen, Apparate und Komponenten“, nach denen eine „Ansammlung von Flüssigkeiten zu vermeiden ist.“
Wie ist nach diesen Vorgaben dieses Handwaschbecken zu bewerten?
- Die gewählten Materialien sind glatt, undurchlässig und beständig gegen reinigungs- und Desinfektionsmittel, also geeignet. Es muss nicht zwingend Edelstahl sein.
- Das Handwaschbecken verfügt über Fertigungsradien r > 3mm, welche eine leichte Reinigung ermöglichen.
- Das Becken hat im Bereich der Armatur eine horizontale Fläche, die eine Ansammlung von Flüssigkeit zulässt; da diese Fläche jedoch leicht zu reinigen ist, kann auch dieser Aspekt akzeptiert werden.
- Das Handwaschbecken hat ein Überlaufloch, welches in einen nicht kontrollier- und reinigbaren Innenbereich führt. In diesen Innenbereich kommen über das Überlaufloch Partikel, Schmutz und Feuchtigkeit und bilden dort einen idealen Bereich für Keimwachstum: ein absolutes NO-GO!
- Das Waschbecken hat einen Ablauf, der nicht verschließbar ist. Unter diesem Ablauf befindet sich der Siphon, in dem ähnliche Zustände herrschen wie hinter dem Überlaufloch. Diese Flüssigkeit im Geruchsverschluss ist jedoch zugänglich und kann nach einem Hygieneplan desinfiziert und auf Keimwachstum getestet werden.
- Die Armatur des Handwaschbeckens kann nur manuell bedient werden, indem man den Hebel mit der Hand betätigt. Dieser Vorgang ist ebenfalls sehr kritisch, da auf der Oberfläche ungewaschener Hände eine Vielzahl unerwünschter Keime ist, welche nun über die Armatur auf weitere Personen übertragen werden können. Ein Design einer solchen Armatur ist daher abzulehnen.
FAZIT: Diesem Waschbecken darf für einen Reinraumbereich keine Freigabe erteilt werden!
Weiterführende Fachliteratur:
1. EU-GMP-Guide to good manufacturing practice; European Commission 2010 Brüssel
2. DIN EN ISI 14644: Reinräume und zugehörige Reinraumbereiche; Beuth Verlag Berlin
3. VDI 2083 Reinraumtechnik; Beuth Verlag Berlin
4. ISPE Baseline Vol. 1: Active pharmaceutical ingredients; ISPE Tampa
5. DIN EN 1672: Nahrungsmittelmaschinen, Allgemeine Gestaltungsleitsätze; Beuth Verlag Berlin
6. EHEDG Doc. 8: Gestaltungskriterien für hygienegerechte Maschinen, Apparate und Komponenten; EHEDG Frankfurt
7. DIN EN ISO 14159: Hygieneanforderungen an die Gestaltung von Maschinen; Beuth Verlag Berlin
8. DIN EN ISO 846: Einwirkung von Mikroorganismen auf Kunststoffe; Beuth Verlag Berlin
9. VDI 6022: Raumlufttechnik, Raumluftqualität; VDI-Verlag Düsseldorf
